Asetýlen, undirbúningur, eignir, efnahvörf

Asetýlen, undirbúningur, eignir, og efnahvörf.
Asetýlen, C2H2 - lífræn efni flokkur, alkynes, ómettuð kolvetni.
Asetýlen, uppskrift, bensín, forskrift, einkenni
Líkamlegir eiginleikar asetýlen
Efnafræðilegir eiginleikar asetýlen
Framleiðsla á asetýleni í iðnaði og rannsóknarstofum
Sprengifimleiki asetýlen og öryggi við meðhöndlun
Asetýlen, uppskrift, bensín, lögun:
Asetýlen (líka - jene) - flokkur lífrænna efna, alkynes, ómettað kolvetnisem samanstendur af tveimur kolefnisatómum og tveimur vetnisatómum.
Efnið formúla asetýlen er C2H2. Uppbyggingarformúla asetýlen, CH≡CH. Isomers hefur ekki.
Uppbygging asetýlen sameindar:
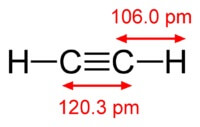
Asetýlen hefur þrefalt samband milli atóma af kolefni.
Asetýlen - litlaust gas, án smekk og lyktar. Hins vegar, tæknilega asetýlenið inniheldur óhreinindi - fosfór vetni, brennisteinsvetni, o.s.frv., sem gefa henni skarpa lykt.
Auðveldara loft. Þéttleiki miðað við þéttleika loftsins af 0.9.
Mjög eldfimt bensín. Eldfimt og sprengiefni.
Asetýlen er meðal fárra efnasambanda, brennslu og sprengingu sem er möguleg í fjarveru af súrefni eða önnur oxunarefni.
Blöndur af asetýleni með loft er sprengifimt í mjög víðtækum styrkleika. Sprengihætta minnkar þegar þynnt asetýlen önnur lofttegundir, til dæmis köfnunarefni, metan eða própan.
Asetýlen krefst mikillar varúðar við meðhöndlun. Getur sprungið úr áfalli, þegar hitað að 500 ° C eða þegar þjappað er að ofan 0.2 MPa við stofuhita. Straumur af asetýleni sem sleppt er úti loft, getur kviknað frá minnsta neista, þar með talin truflanir rafmagns frá fingri. Geymsla á asetýleni með sérstöku strokkafyllt með porous efni sem er bleytt með asetoni. Þeir asetýlen er geymt í lausn með asetoni.
Lítið leysanlegt í vatn. Mjög leysanlegt í asetoni. Leysanlegt í öðrum lífrænum efnum (bensín, bensen, o.s.frv.)
Asetýlen hefur smá eituráhrif.
Líkamlegir eiginleikar asetýlen:
| Heiti breytu: | Gildi: |
| Litur | án litar |
| Lyktin | lyktarlaust |
| Bragð | enginn smekkur |
| Samanlagt ríki (kl 20 ° C og andrúmsloftþrýstingur af 1 Hraðbanki.) | bensín |
| Þéttleiki (kl 20 ° C og andrúmsloftþrýstingur af 1 Hraðbanki.) kg / m3 | 1,0896 |
| Þéttleiki (kl 0 ° C og andrúmsloftþrýstingur af 1 Hraðbanki.) kg / m3 | 1,173 |
| Bræðslumark, ° C | -80,8 |
| Suðumark, ° C | -80,55 |
| Þrefaldur punktur, ° C | 335 |
| Sjálfkveikjuhitinn, ° C | 335 |
| Sjálfkveikjuþrýstingur, MPa | 0,14-0,16 |
| Mikilvægt hitastig *, ° C | Af 35.94 |
| Gagnrýninn þrýstingur, MPa | 6,26 |
| Sprengistyrkur blöndunnar af gasi við loft, % miðað við rúmmál | 2.1 til 100 |
| Sérstakur brennsluhiti, MJ / kg | 56,9 |
| Logi hitastig, ° C | 3150-3200 |
| Molamessa, g / mól | 26,038 |
* við hitastig yfir afgerandi hitastigi bensínið ekki hægt að þétta við neinn þrýsting.
Efnafræðilegir eiginleikar asetýlen:
Efnafræðilegir eiginleikar asetýlen eru svipaðir eiginleikum annarra fulltrúa fjölda alkynna. Svo það einkennist af eftirfarandi efnahvörfum:
1. galogenirovannami asetýlen:
CH≡CH + Br2 → CHBr = CHBr (1,2-díbrómetan);
CHBr = CHBr + Br2 → CHBr2-CHBr2 (1,1,2,2-tetrabrómetan).
Viðbrögðin halda áfram stigum með myndun afleiðna af alkanum.
Meðan á þessum viðbrögðum stendur, asetýlen mislit bróm vatn.
2. vatnshalogenering asetýlen:
CH≡CH + HBr → CH2 = CHBr (brómat).
3. vökvun asetýlen (viðbrögð Michael G. Kucherov, 1881):
CH≡CH + H2O → [CH2 = CH-OH] (enol) → CH3-CH = O (asetaldehýð ) (kat = HgSO4, Hg(NO3)2).
4. trimerization á asetýleni (viðbrögð Nikolaya Dmitrievicha zelinskogo, 1927):
3СН≡CH → C6H6 (bensen) (kat = virk kolefni, til = 450-500 ÞAÐ).
Viðbrögðin við snyrtingu á asetýleni eru sérstakt tilfelli viðbragðsins af fjölliðun asetýlen á sér stað með því að láta asetýlen yfir virkjað kol við hitastig 450-500 ÞAÐ.
5. dimerization asetýlen:
CH≡CH + CH2CH → CH2 = CH-C6CH (fengið vínýlasetýlen) (kat = vatnslausn af CuCl og NH 4 CL).
Viðbrögð dimerization asetýlen eru sérstakt tilfelli viðbragða af fjölliðun asetýlen.
6. brennslu asetýlen:
2SN≡CH + 5О2 → 4СО2 + 2Н2О.
Asetýlen brennur með hvítum björtum loga.
7. oxun asetýlen.
Viðbrögðin og afurðir þeirra eru ákvörðuð af því umhverfi sem þau eiga sér stað í.
8. endurheimt asetýlen:
CH≡CH + H2 → C2H4 (etýlen) (kat = Ni, Pd eða Pt, aukið til);
CH≡CH + 2H2 → C2H6 (etan) (kat = Ni, Pd eða Pt, aukið til).
Framleiðsla á asetýleni í iðnaði og rannsóknarstofu. Efnahvarf - jöfnu asetýlen:
Asetýlen á rannsóknarstofu er afleiðing eftirfarandi efnahvarfa:
1. verkun vatns á kalsíumkarbíði:
CaC2 + H2O → CA(Ó)2 + C2H2.
2. ofvötnun metans:
2CH4 → C2H2 + 3H2 (háð > 1500 OC).
3. ofvötnun etýlen:
CH2 = CH2 → CH≡CH + H2 (kat = Pt, Ni, Al2O3, Cr2O3, til = 400-600 ° C).
Asetýlen í greininni fá á eftirfarandi hátt og aðferðir:
4. karbít aðferð:
Fáðu fyrst kalk úr kalsíumkarbónati.
CaCO3 → Há + CO2. (til = 900-1200 oC).
Fáðu þér þá karbít af kalsíum, fusing kalsíumoxíð og kók í rafmagnsofni við hitastig 2500-3000 ° C.
Hár + 3C → CaC2 + CO. (til = 2500-3000 ÞAÐ).
Frekari, kalsíumkarbíð er meðhöndlað með vatni við þekkt viðbrögð.
CaC2 + H2O → CA(Ó)2 + C2H2.
Niðurstaðan er að asetýlen með mikla hreinleika er 99.9 %.
5. háhitasprunga metans:
Háhitasprunga metans er framkvæmd samkvæmt þekktum viðbrögðum degidrirovaniya metans í rafbogaofni við hitastig 2000-3000 ° C og spenna milli rafskautanna í 1000 V. framleiðsla asetýlen er 50 %.
6. hinar ýmsu aðferðir við pyrolysis af metani:
Tegund háhitasprungu á metani eru endurnýjunarflæði (Wulff ferli), oxandi pyrolysis (Sachs-ferli eða BASF ferli), einsleita pyrolysis, pyrolysis í miðlungs lágum hita plasma.
Þannig, meðan á endurnýjun sótthreinsunar stendur, brenna fyrst metan og hita upp stútinn ofnsins til 1350-1400 ° C. Síðan í gegnum hitaða stút til að skera burt flæði metansins, þannig að mynda asetýlen.
Þegar oxað er pyrolysis af metani er blandað við súrefni og brennt. Hitinn sem myndast veldur því að hita afganginn af metaninu upp í 1600 ° C, sem digidrive í asetýleni. Uppskeran af asetýleni er 30-32 %.
Við einsleita pírolysu metans og súrefnis er brennt inn í ofni við hitastig 2000 ° C. Þá, forhitað til 600 ° C, afgangurinn af metaninu fer í gegnum ofninn, þannig að mynda asetýlen.
Við kyrrsetningu í umhverfi með lágan hita plasma metan er hitað með þotu af jónuðu gasi (argon eða vetni).
Notkun og notkun asetýlen:
- sem hráefni í efnaiðnaði til framleiðslu ediksýru, etýlalkóhól, leysiefni, plast, tilbúið gúmmí, arómatísk kolvetni,
- til gassuðu og skurðar málma,
- fyrir tæknilegt kolefni,
- sem uppspretta mjög björt, hvítt ljós í Autonomous lampar, þar sem það fæst með hvarfinu á kalsíumkarbíði og vatni.
Sprengifimleiki asetýlen og öryggi við meðhöndlun:
Asetýlen hefur sprengifimleika.
Þess vegna, meðferð með asetýleni krefst þess að farið sé að öryggisreglum.
Asetýlen brennur og springur jafnvel án súrefnis og annarra oxunarefna.
Blöndur af asetýleni með lofti eru sprengiefni í mjög fjölbreyttum styrk.
Þota af asetýlenisleppt undir berum himni, getur kviknað frá minnsta neista, þar með talin truflanir rafmagns frá fingri.
Vzryvaet asetýlen veltur á mörgum þáttum: þrýstingur, hitastig, hreinleiki asetýlen, innihald raka, tilvist hvata og annarra efna og af öðrum ástæðum.
Kveikjuhiti asetýlen við venjulegan - loftþrýsting á bilinu 500-600 ° C. Þegar þrýstingur lækkar íkveikjuhita asetýlen. Þannig, við þrýsting á 2 kgf / cm2 (0.2 MPa, 1,935682 Hraðbanki.) kveikjuhiti asetýlen er jafnt og 630 ° C. Og við þrýsting á 22 kgf / cm2 (2.2 MPa, 21,292502 Hraðbanki.) kveikjuhiti asetýlen jafnt og 350 ° C.
Tilvist asetýlen agna mismunandi efna eykur snertingu við yfirborðið og dregur þannig úr kveikjuhita við lofthjúp. Til dæmis, virkt kolefni lækkar kveikjuhita asetýlen í 400 ° C, vatnið af járnoxíði (ryð) - allt að 280-300 ° C, járnspænir - allt að 520 ° C, koparspænir upp að 500-520 ° C, karbít af kalsíum, allt að 500 ° C, áloxíð - allt að 490 ° C, kopar spænir - 460 ° C, járnoxíðið - 280 ° C, koparoxíð upp að 250 ° C.
Sprengifimleiki asetýlen lækkar við þynningu asetýlen með öðru lofttegundir, til dæmis köfnunarefni, metan eða própan.
Við vissar aðstæður bregst asetýlen við kopar, silfur og kvikasilfur til að mynda sprengiefni. Þess vegna, við framleiðslu á asetýlenbúnaði (t.d., lokar, strokka) ekki nota málmblöndursem innihalda meira en 70 % Með.
Geymsla og flutningur á asetýleni, með sérstökum stálhólkum hvítum lit. (með rauðri áletrun “A”) fyllt með óvirkum porous efni (t.d., kol). Þannig asetýlen er geymt og flutt í þessum pokum í formi lausnar af asetýleni í asetoni undir þrýstingi 1.5-2.5 MPa.
Athugið: © mynd //www.pexels.com, //Pixabay.com



